| Официальное полное имя |
Рекомбинантный фактор некроза опухоли человека-альфа / TNFSF2 GMP (rHuTNF-альфа / TNFSF2) |
| Последовательность |
 |
| Аминокислотная последовательность |
MVRSSSRTPS DKPVAHVVAN PQAEGQLQWL NRANALLAN GVELRDNQLV VPSEGLYLIY SQVLFKGQGC PSTHVLLTHT ISRIAVSYQT KVNLLSAIKS PCQRETPEGA EAKPWYEPYIN DGGRLGLIIDQLEKG |
| Синонимы |
Фактор некроза опухоли, TNFSF2, кахектин, фактор, вызывающий дифференцировку, DIF, некрозин, цитотоксин |
| Номер доступа |
P01375 |
| GeneID |
7124 |
| Обзор |
Фактор некроза опухоли альфа (TNF-альфа), также называемый кахектином, является наиболее известным членом семейства TNF, который может вызывать гибель клеток. Этот белок продуцируется нейтрофилами, активированными лимфоцитами, макрофагами, NK-клетками, LAK-клетками, эндотелиальными клетками астроцитов, гладкомышечными клетками и некоторыми трансформированными клетками. TNF-альфа встречается в секретируемой растворимой форме и в форме заякоренной мембраны, оба из которых являются биологически активными. Встречающаяся в природе форма TNF-альфа гликозилирована, но негликозилированный рекомбинантный TNF-альфа имеет сопоставимую биологическую активность. Сообщается, что биологически активная нативная форма TNF-альфа представляет собой тример. Человеческий и мышиный TNF-альфа демонстрируют примерно 79% гомологии на уровне аминокислот и перекрестной реактивности между двумя видами. Были описаны два типа рецепторов для TNF-альфа, и практически все изученные типы клеток показывают присутствие одного или обоих этих типов рецепторов. |
| Источник |
Кишечная палочка. |
| Молекулярная масса |
Примерно 17.5 кДа, одна негликозилированная полипептидная цепь, содержащая 158 аминокислот. |
| Биологическая активность |
Полностью биологически активный по сравнению со стандартом. ED50, определенная с помощью анализа цитотоксичности с использованием мышиных клеток L929, составляет менее 0.05 нг / мл, что соответствует удельной активности> 2.0 × 107 МЕ / мг в присутствии актиномицина D. |
| Внешний вид |
Стерильный фильтрованный белый лиофилизированный (лиофилизированный) порошок. |
| Формулировка |
Лиофилизирован из концентрированного раствора, профильтрованного через 0.2 мкм, в 10 мМ PB, 10 мМ NaCl, pH 7.0. |
| эндотоксин |
Менее 0.01 EU / мкг rHuTNF-α / TNFSF2 GMP, как определено методом LAL. |
| Восстановление |
Мы рекомендуем кратковременно центрифугировать этот флакон перед открытием, чтобы довести содержимое до дна. Развести в стерильной дистиллированной воде или водном буфере, содержащем 0.1% BSA, до концентрации 0.1–1.0 мг / мл. Исходные растворы следует разделить на рабочие аликвоты и хранить при температуре ≤ -20 ° C. Дальнейшие разведения следует проводить в соответствующих буферных растворах. |
| Стабильность и хранение |
Используйте морозильную камеру для ручного размораживания и избегайте повторяющихся циклов замораживания-оттаивания. - Минимум 12 месяцев при хранении при температуре ≤ -20 ° C при поставке. См. Сертификат подлинности партии для использования по дате. - 1 месяц, от 2 до 8 ° C в стерильных условиях после восстановления. - 3 месяца, от -20 до -70 ° C в стерильных условиях после восстановления. |
| Рекомендации |
1. Давенпорт С., Кенни Х., Эшли Д.Т. и др. 2012. Eur J Clin Invest, 42: 1173-9.2. Кавальканти Ю.В., Брелаз М.К., Невес Дж.К. и др. 2012. Пулм Мед, 2012: 745483.3. Шэн В.С., Ху С., Ни Х.Т. и др. 2005. Дж. Лейкоц Биол, 78: 1233-41.4. Бертольд-Лослебен МандХиммерих Х. 2008. Curr Neuropharmacol, 6: 193-202. |
| SDS-СТРАНИЦА |
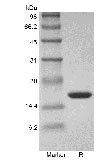 |
| Паспорт безопасности (SDS) Скачать |
Нажмите, чтобы скачать |
| Технический паспорт (TDS) Скачать |
Нажмите, чтобы скачать |



