| Официальное полное имя |
Рекомбинантный фактор некроза опухоли человека-альфа / TNFSF2, вариант (rHuTNF-alpha / TNFSF2, вариант) |
| Последовательность |
 |
| Аминокислотная последовательность |
MRKRKPVAHV VANPQAEGQL QWLNRRANAL LANGVELRDN QLVVPSEGLY LIYSQVLFKG QGCPSTHVLL THTISRIAVS YQTKVNLLSA IKSPCQRETP EGAEAKPWYE PIYLGGRLSYLDI |
| Синонимы |
Фактор некроза опухоли, TNFSF2, кахектин, фактор, индуцирующий дифференцировку (DIF), некрозин, цитотоксин |
| Номер доступа |
P01375 |
| GeneID |
7124 |
| Обзор |
Клиническое применение мощного противоопухолевого действия TNF-альфа уже проводилось. limited провоспалительными побочными эффектами, включая лихорадку, ограничивающую дозу гипотензию, гепатотоксичность, внутрисосудистый тромбоз и кровотечение. Разработка клинически применимых альфа-мутантов TNF с низкой системной токсичностью представляет большой фармакологический интерес. Человеческий TNF-альфа, который связывается с мышиным TNF-R55, но не с мышиным TNF-R75, проявляет сохраненную противоопухолевую активность и сниженную системную токсичность у мышей по сравнению с мышиным TNF-альфа, который связывается с обоими мышиными рецепторами TNF. На основе этих результатов было разработано множество альфа-мутантов TNF, которые избирательно связываются с TNF-R55. Эти мутанты проявляли цитотоксическую активность в отношении линий опухолевых клеток in vitro и проявляли более низкую системную токсичность in vivo. |
| Источник |
Кишечная палочка. |
| Молекулярная масса |
Примерно 16.9 кДа, одна негликозилированная полипептидная цепь, содержащая 151 аминокислоту. По сравнению с диким типом, вариант rHuTNF-α имеет делецию аминокислотной последовательности (аа) из аминокислотных остатков 1-7, и следующие аминокислотные остатки заменяют Arg8, Lys9, Arg10 и Phe157, которые, как доказано, обладают большей активностью и меньшей воспалительной стороной. эффект in vivo. |
| Биологическая активность |
Полностью биологически активный по сравнению со стандартом. ED50, определенная с помощью анализа цитотоксичности с использованием мышиных клеток L929, составляет менее 0.01 нг / мл, что соответствует удельной активности> 1.0 × 107 МЕ / мг в присутствии актиномицина D. |
| Внешний вид |
Стерильный фильтрованный белый лиофилизированный (лиофилизированный) порошок. |
| Формулировка |
Лиофилизирован из отфильтрованного 0.2 мкм концентрированного раствора в PBS, pH 7.0. |
| эндотоксин |
Менее 1 EU / мкг rHu TNF-α / TNFSF2, вариант, определенный методом LAL. |
| Восстановление |
Мы рекомендуем кратковременно центрифугировать этот флакон перед открытием, чтобы довести содержимое до дна. Развести в стерильной дистиллированной воде или водном буфере, содержащем 0.1% BSA, до концентрации 0.1–1.0 мг / мл. Исходные растворы следует разделить на рабочие аликвоты и хранить при температуре ≤ -20 ° C. Дальнейшие разведения следует проводить в соответствующих буферных растворах. |
| Стабильность и хранение |
Используйте морозильную камеру для ручного размораживания и избегайте повторных циклов замораживания-оттаивания. - 12 месяцев с даты получения, от -20 до -70 ° C в состоянии поставки. - 1 месяц, от 2 до 8 ° C в стерильных условиях после восстановления. - 3 месяца, От -20 до -70 ° C в стерильных условиях после восстановления. |
| Рекомендации |
|
| SDS-СТРАНИЦА |
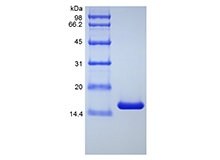 |
| Паспорт безопасности (SDS) Скачать |
Нажмите, чтобы скачать |
| Технический паспорт (TDS) Скачать |
Нажмите, чтобы скачать |



